Farmacogenética: cuando tu ADN guía tu tratamiento
Imagina que dos personas toman el mismo medicamento, en la misma dosis, para el mismo problema… y una mejora rápidamente mientras la otra sufre efectos secundarios. Esta situación real no es casualidad, sino que tiene una base biológica.
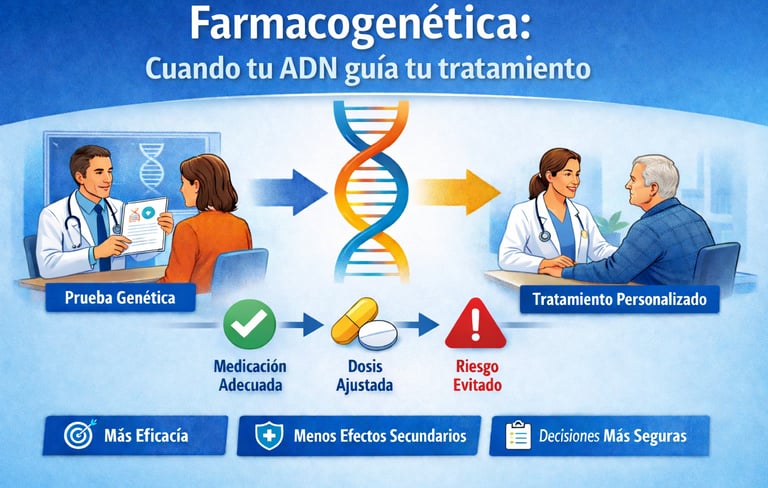
¿Qué es la farmacogenética?
La farmacogenética estudia cómo nuestras diferencias genéticas influyen en la forma en que respondemos a los medicamentos. Y está cambiando la forma de prescribir.
Es una herramienta de la medicina personalizada que ayuda a responder tres preguntas clave antes de empezar un tratamiento:
¿Este medicamento funcionará bien en esta persona?
¿Necesita una dosis diferente?
¿Existe riesgo elevado de efectos adversos?
Organizaciones como el Clinical Pharmacogenetics Implementation Consortium y la Dutch Pharmacogenetics Working Group elaboran guías para ayudar a los profesionales sanitarios a utilizar la información genética cuando ya está disponible. Por su lado, la U.S. Food and Drug Administration y la ClinPGx publican listados de medicamentos cuyo etiquetado incluye información genética relevante.
¿Qué cambia para los pacientes?
Se estima que entre un 30 % y un 50 % de los pacientes no responden adecuadamente a determinados tratamientos estándar, dependiendo del área terapéutica. En oncología o psiquiatría, la variabilidad interindividual es especialmente relevante.
Además, las reacciones adversas a medicamentos (RAM) siguen siendo un problema de salud pública. En Europa y EE. UU., se calcula que provocan entre el 3 % y el 7 % de las hospitalizaciones, y en pacientes hospitalizados pueden afectar hasta al 10 % de ellos. Muchas de estas reacciones están relacionadas con diferencias en el metabolismo de los fármacos.
Aquí es donde la farmacogenómica marca la diferencia.
1️⃣ Tratamientos más ajustados a la biología individual
Algunas variantes genéticas influyen directamente en cómo el organismo metaboliza medicamentos. Por ejemplo, ciertos genes del sistema enzimático hepático pueden hacer que una persona elimine un fármaco demasiado rápido (disminuyendo su eficacia) o demasiado lento (aumentando el riesgo de toxicidad).
En términos prácticos, esto puede significar:
Elegir un fármaco alternativo desde el inicio.
Ajustar la dosis antes de que aparezcan problemas.
Evitar semanas o meses de prueba y error.
Para el paciente, esto se traduce en menos incertidumbre y más probabilidad de acierto desde la primera prescripción.
2️⃣ Menor probabilidad de efectos adversos graves
Algunas asociaciones gen–fármaco están bien documentadas y permiten prevenir reacciones graves antes de que ocurran. En determinados tratamientos, la identificación previa de una variante genética de riesgo puede reducir de forma significativa la probabilidad de toxicidad severa. En contextos específicos, el cribado genético ha demostrado disminuir eventos adversos graves asociados a ciertos medicamentos.
El impacto es, por tanto, clínico y humano. Evitar una reacción adversa grave significa evitar ingresos hospitalarios, secuelas y ansiedad innecesaria.
3️⃣ Más confianza y mejor adherencia
Cuando el paciente sabe que su tratamiento ha sido ajustado teniendo en cuenta su perfil biológico, aumenta la percepción de personalización y seguridad. Diversos estudios muestran que la confianza en la terapia influye directamente en la adherencia. Y sabemos que la falta de adherencia puede reducir la efectividad terapéutica hasta en un 50 % en enfermedades crónicas.
La farmacogenética no elimina todos los riesgos, pero sí reduce la variabilidad no controlada.
¿Qué cambia para el sistema sanitario?
La farmacogenómica no es solo una prueba genética, es un rediseño del proceso de prescripción y esto implica gran parte de estrategia.
1️⃣ Menos eventos adversos evitables
Las reacciones adversas a medicamentos suponen un coste significativo para los sistemas sanitarios, estimando que representan miles de millones de euros anuales en costes directos e indirectos.
Reducir hospitalizaciones asociadas a toxicidad mejora tanto resultados clínicos como la liberación de recursos asistenciales. Un modelo preventivo siempre es más eficiente que uno reactivo.
2️⃣ Integración de datos en la historia clínica
El verdadero valor aparece cuando el resultado genético se integra estructuradamente en la historia clínica electrónica, activando alertas automáticas en el momento de prescribir y, a su vez, permanece disponible durante toda la vida del paciente. Esto exige interoperabilidad, gobernanza del dato y soporte a la decisión clínica.
El dato genético es, en la mayoría de los casos, estable a lo largo del tiempo. Una sola prueba puede informar múltiples decisiones terapéuticas futuras.
3️⃣ Cumplimiento normativo y protección de datos
La información genética es un dato de categoría especial según el General Data Protection Regulation, por lo que su tratamiento requiere garantías reforzadas de seguridad, trazabilidad y control de acceso. Además, cuando intervienen sistemas de ayuda a la decisión basados en algoritmos, pueden activarse requisitos regulatorios adicionales en el marco del Reglamento europeo de productos sanitarios o del Reglamento europeo de inteligencia artificial.
4️⃣ Equidad y acceso
Un desafío clave es evitar que la medicina personalizada aumente desigualdades. Si determinadas poblaciones no están adecuadamente representadas en estudios genéticos, el beneficio puede no distribuirse de forma equitativa.
La implementación debe ir acompañada de políticas públicas que garanticen acceso progresivo y sostenible.
Un caso clínico: el corazón y el medicamento adecuado
Un paciente que ha sufrido un evento cardiovascular y necesita un fármaco antitrombótico para evitar que vuelva a ocurrir. En la mayoría de los casos, el tratamiento funciona bien. Pero en algunas personas, el organismo no activa correctamente el medicamento debido a una variante genética. El resultado: menor protección y mayor riesgo.
Hoy, en determinados contextos clínicos, puede realizarse una prueba genética sencilla que indica cómo metaboliza el fármaco antitrombótico (p.ej., clopidogrel), ya que hay variantes que pueden reducir la activación del fármaco y, por tanto, su efecto. En estos escenarios, una estrategia de farmacogenética puede guiar alternativas terapéuticas o vigilancia, ya que existe una decisión más informada.
Para el sistema sanitario, significa menos complicaciones evitables.
La farmacogenética demuestra que la medicina personalizada no es una idea abstracta, sino una realidad que empieza en el ADN y termina en la decisión clínica. Cuando estos datos genéticos, gracias a los gemelos digitales, se integran con información clínica y contextual, se consigue simular escenarios terapéuticos antes de aplicarlos al paciente real, anticipando respuestas, optimizando tratamientos y reduciendo riesgos. En Luperca Médica trabajamos precisamente en esa convergencia entre datos, simulación y práctica clínica, para convertir la medicina personalizada en una herramienta operativa, segura y escalable dentro del sistema sanitario.


